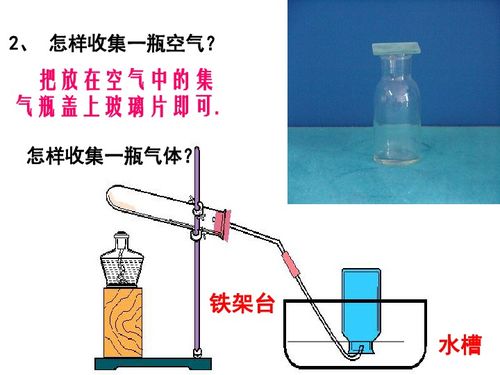
氣體制備、凈化與收集 實驗室操作全解析
在化學實驗室中,氣體的制備、凈化和收集是基礎且關鍵的實驗操作。掌握這一系列流程的原理與方法,是進行后續性質研究或實際應用的前提。本文將系統性地闡述這三個環節的核心要點。
一、氣體制備:方法與選擇
氣體制備的核心是根據所需氣體的化學性質,選擇合適的反應原理和發生裝置。主要方法包括:
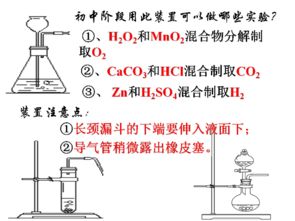
- 固體加熱法:適用于熱穩定性較差、受熱易分解的固體反應物,如加熱高錳酸鉀制取氧氣(2KMnO? → K?MnO? + MnO? + O?↑)。常用裝置為帶有酒精燈和導管的硬質玻璃管。
- 固液常溫法:這是最常用的方法,適用于塊狀或顆粒狀固體與液體在不加熱條件下反應,如鋅粒與稀硫酸反應制取氫氣(Zn + H?SO? → ZnSO? + H?↑)。常用裝置為簡易啟普發生器或其變體。
- 液液加熱法:適用于兩種或多種液體需要加熱才能順利反應的體系,如乙醇與濃硫酸在170℃下反應制備乙烯。此時需使用帶有溫度計和分液漏斗的圓底燒瓶裝置。
選擇依據:首要考慮反應物的狀態和反應條件(是否需要加熱),其次是反應速率可控性、安全性以及裝置簡易程度。
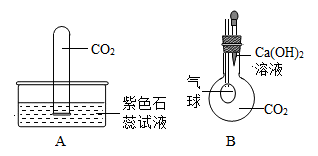
二、氣體凈化:除去雜質
由于反應物不純、副反應或裝置帶入水汽等原因,生成的氣體常含有雜質。凈化目的就是獲得純凈的目標氣體。凈化操作通常在制備之后、收集之前進行,通過洗氣瓶或干燥管實現。
- 除雜原則:
- 不減少:凈化試劑不能與目標氣體發生反應。
- 不引入:不能引入新的雜質氣體。
- 易分離:最好通過一次洗氣或干燥即可完成。
- 常見凈化試劑與方法:
- 除酸性雜質(如HCl、CO?、SO?):可用堿性溶液(如NaOH溶液)或固體堿石灰。
- 除堿性雜質(如NH?):可用酸性溶液(如稀硫酸)。
- 除還原性雜質(如H?S):可用硫酸銅溶液或高錳酸鉀溶液。
- 除水蒸氣(干燥):根據氣體性質選擇干燥劑。酸性干燥劑(如濃硫酸、五氧化二磷)不能干燥堿性氣體(如NH?);堿性干燥劑(如堿石灰、固體NaOH)不能干燥酸性氣體(如CO?、SO?、HCl);中性干燥劑(如無水氯化鈣)應用較廣,但不能干燥NH?。
操作順序:一般先除雜后干燥。若用水溶液除雜,氣體出來時會帶出水蒸氣,因此干燥必須放在最后一步。
三、氣體收集:依據性質定方法
收集方法的選擇完全取決于氣體本身的物理和化學性質。
- 排水集氣法:
- 適用氣體:不易溶于水且不與水反應的氣體,如O?、H?、N?、CO、CH?等。
- 優點:收集到的氣體純度高、濃度大。
- 操作:集氣瓶裝滿水倒扣在水槽中,導管伸入瓶口。
- 向上排空氣法:
- 適用氣體:密度大于空氣(平均分子量 > 29)且不與空氣中成分反應的氣體,如CO?、SO?、HCl、Cl?(通常用排飽和食鹽水法更好)等。
- 操作:導管伸入集氣瓶底部,利用氣體密度大而下沉,將空氣從瓶口向上排出。
- 向下排空氣法:
- 適用氣體:密度小于空氣(平均分子量 < 29)且不與空氣中成分反應的氣體,如H?、NH?、CH?等。
- 操作:導管伸入集氣瓶底部,利用氣體密度小而上升,將空氣從瓶口向下排出。
注意事項:排空氣法收集氣體時,導管應盡可能伸到集氣瓶底部,以利于排盡空氣;同時可在瓶口進行驗滿操作。
四、實驗流程整合與安全
一個完整的氣體制備實驗,需將上述三個環節有序串聯:發生裝置 → 凈化裝置 → 干燥裝置 → 收集裝置。若氣體有毒或有害(如Cl?、SO?),必須在最后連接尾氣處理裝置(如用NaOH溶液吸收)。
安全始終是第一要務。實驗前必須明確氣體的毒性、可燃性、爆炸極限等;檢查裝置氣密性;加熱反應時防止液體倒吸;易燃易爆氣體(如H?)收集或實驗時需遠離明火。
氣體制備、凈化與收集是一個環環相扣的系統工程。深入理解每一步的原理,并嚴格遵循操作規范,是實驗成功與人員安全的根本保障。
如若轉載,請注明出處:http://m.bpwei.cn/product/70.html
更新時間:2026-04-08 14:52:51